Le virus de l’hépatite C (HCV ou VHC) découvert en 1988 est un virus strictement humain à tropisme hépatique responsable d’hépatites aiguës et chroniques pouvant évoluer vers une cirrhose et un hépatocarcinome.
CARACTÉRISTIQUES VIROLOGIQUES
TAXONOMIE
Le virus de l’hépatite C appartient à la famille des Flaviviridae et au genre Hepacivirus se répartissant en 8 génotypes (1 à 8). Le HCV est un virus enveloppé de taille moyenne (40–50 nm) de forme sphérique.
GÉNOME
Le génome du HCV est composé d’un ARN (acide ribonucléique) simple brin de polarité positive de 9,6 kb (figure III.9.1). L’ARN viral contient un cadre de lecture unique flanqué à ses deux extrémités par des séquences non codantes (NC) de longueurs variables, les régions 5’NTR et 3’NTR. Ce cadre de lecture code pour une polyprotéine précurseur unique d’environ 3 000 acides aminés qui, après clivage par des protéases cellulaires et virales, donne naissance aux protéines structurales et aux 7 protéines non structurales.

PROTÉINES VIRALES
Les protéines structurales Core forment les constituants de la capside et les protéines E1 et E2 de l’enveloppe virale jouent un rôle majeur dans le processus d’entrée du virus dans les cellules. Les protéines non structurales p7, NS2, NS3-4A, NS4B, NS5A et NS5B sont impliquées dans le clivage de la polyprotéine et dans la réplication virale. Les derniers traitements du HCV (agents antiviraux directs ou AAD) ciblent certaines de ces protéines virales non structurales.
TROPISME ET RÉPLICATION
Le cycle de réplication du HCV se déroule exclusivement dans le cytoplasme des hépatocytes. Après la libération dans le cytoplasme, le génome viral est directement traduit en protéines. Le complexe de réplication nécessite plusieurs protéines virales non structurales, dont la protéase NS3 et son cofacteur NS4A, la protéine NS5A et l’ARN polymérase ARN dépendante NS5B.
Un ARN simple brin de polarité négative complémentaire de l’ARN viral est synthétisé. Celui-ci sert de matrice pour la synthèse de nombreuses molécules d’ARN viral de polarité positive. Ces ARN nouvellement synthétisés serviront alors de matrice pour la traduction en protéines virales ou seront encapsidés pour former de nouveaux virions. L’infection est caractérisée par des niveaux élevés de production virale avec des charges virales dans le sang (virémie) entre 4 et 7 log10 copies/mL. Ce haut niveau de réplication associé aux erreurs générées par la polymérase virale, qui ne possède pas d’activité de correction (proofreading), ont pour conséquence une variabilité importante pour ce virus.
La détermination des génotypes viraux n’est plus d’une importance majeure en vue du traitement des personnes infectées puisque la plupart des nouveaux traitements sont efficaces, quel que soit le génotype ou le sous-type viral.
| Points clés Le HCV est un virus strictement humain à tropisme hépatique présentant une forte variabilité génomique. |
DONNÉES ÉPIDÉMIOLOGIQUES
Le HCV se transmet par le sang et la contamination est principalement parentérale : par transfusion avant 1990, principalement par toxicomanie désormais, ou via des pratiques à risque sans conditions d’hygiène (tatouages, piercings). La contamination est possible mais rare lors de rapports sexuels traumatiques ou de la mère à l’enfant.
La prévalence mondiale est estimée à 1 % avec environ 70 millions de personnes chroniquement infectées et une grande disparité de répartition dans le monde. En France, le nombre de personnes ayant des anticorps dirigés contre le HCV était estimé en 2011 à 350 000, et le nombre de personnes ayant un ARN du HCV à 133 000. L’incidence de l’hépatite C aiguë n’est pas connue car elle est très souvent asymptomatique et il n’existe pas de déclaration obligatoire.
| Points clés Les infections par le HCV sont plus souvent asymptomatiques et sont donc difficilement quantifiables sans réaliser des tests de dépistage ou de diagnostic. |
PHYSIOPATHOLOGIE ET MANIFESTATIONS CLINIQUES
L’infection par ce virus est le plus souvent asymptomatique avec une augmentation sérique de l’alanine aminotransférase (ALAT) constamment présente. Dans 60 à 90 % des sujets, l’infection aiguë n’est pas limitée et évolue vers une hépatite chronique (figure III.9.2).
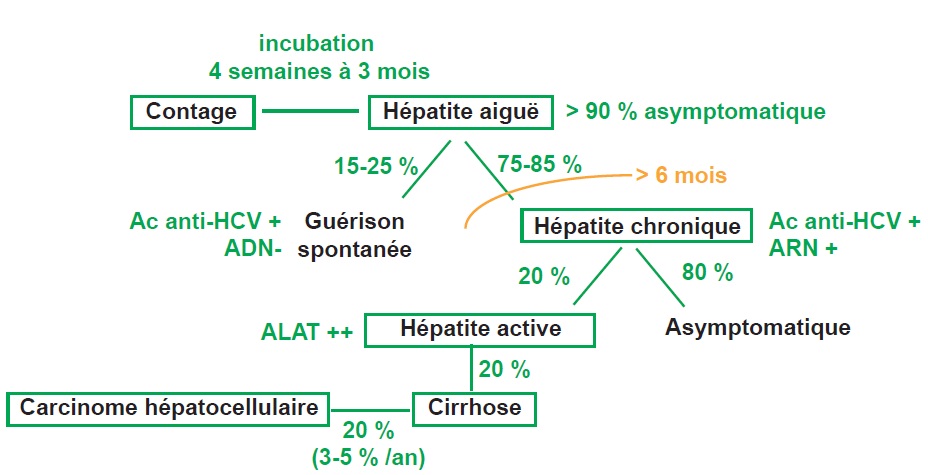
ADN : acide désoxyribonucléique ; ARN : acide ribonucléique ; ALAT : alanine aminotransférase ; HCV : virus de l’hépatite C.
HÉPATITES AIGUËS
Après une incubation de 4 à 12 semaines, l’infection par le virus de l’hépatite C entraîne une hépatite aiguë asymptomatique ou paucisymptomatique. Les valeurs des transaminases (ALAT) peuvent être supérieures à 1 000 UI/mL. Ainsi, l’incidence de ces infections aiguës n’est pas connue et le diagnostic rarement fait à ce stade. Le sujet infecté va développer des anticorps mais généralement ces anticorps ne confèrent pas une immunité protectrice. Le HCV est responsable de façon exceptionnelle d’hépatites fulminantes.
HÉPATITES CHRONIQUES
L’infection persiste chez la majorité des sujets infectés (60 à 90 %) avec la présence d’une activité nécrotique et inflammatoire à bas bruit entraînant une fibrose hépatique. La symptomatologie est essentiellement due à la réponse immunitaire qui va éliminer les hépatocytes infectés.
Une hépatite chronique est définie par la présence d’un marqueur viral direct pendant plus de 6 mois. L’évolution de la maladie est lente en l’absence de comorbidités : 20 à 30 années jusqu’au stade de cirrhose pouvant conduire à un hépatocarcinome. Ce risque est plus important chez les sujets co-infectés par le HIV (virus de l’immunodéficience humaine), les personnes consommant de l’alcool ou ayant une pathologie hépatique sous-jacente.
La maladie suite à une infection chronique par le HCV est quelquefois définie comme une maladie systémique car diverses manifestations extrahépatiques sont rapportées (cryoglobulinémie entraînant des vascularites, glomérulonéphrite, résistance à l’insuline…).
| Points clés L’infection par le HCV est souvent silencieuse et va persister chez la majorité des personnes contaminées qui, en l’absence de traitement, évolueront lentement vers une cirrhose et un hépatocarcinome. |
DIAGNOSTIC
Le diagnostic repose en première intention sur le diagnostic indirect (dépistage HCV) et si celui-ci est positif, sur le diagnostic direct pour permettre la mise en place d’un traitement antiviral et le suivi de la réponse à ce traitement. Puisque l’infection par le HCV est le plus souvent asymptomatique, le dépistage est essentiel dans les populations à risque (usagers de drogues, personnes incarcérées, sujets séropositifs pour le HIV, hommes ayant des relations sexuelles avec des hommes).
DIAGNOSTIC INDIRECT
La fenêtre sérologique entre la contamination et la séroconversion est en moyenne de 60 à 80 jours. Le dépistage biologique de l’infection par le HCV repose sur la détection des anticorps totaux anti-HCV à l’aide d’un test immuno-enzymatique de 3e génération (ELISA [Enzyme Linked Immuno-Sorbent Assay]), à partir d’un échantillon de sang recueilli au pli de coude sur tube sec (sérum).
Deux résultats sont possibles :
▶ résultat négatif sans facteurs de risque d’exposition à une infection lors des 3 derniers mois, il peut être conclu à l’absence de contact avec le virus. Si une situation à risque est évoquée, il est conseillé de réaliser de nouveau ce test dans les 3 prochains mois. Chez les personnes immunodéprimées, la détection des anticorps suite à l’infection est inconstante et il est donc conseillé de rechercher l’ARN génomique du HCV par une méthode directe (RT-PCR [Reverse Transcriptase-Polymerase Chain Reaction]) dans le plasma ;
▶ résultat positif : si le patient n’a pas d’antériorité, le contrôle de cette sérologie est recommandé à l’aide d’un autre réactif sur un second prélèvement. Si la sérologie de contrôle est positive, il est nécessaire de rechercher l’ARN viral afin de différencier une infection active ou une élimination du virus suite à une élimination naturelle (infection aiguë sans infection chronique) ou un traitement.
La détection des anticorps anti-HCV est également possible avec des TROD (tests rapides d’orientation diagnostique) à partir de sang capillaire prélevé au bout du doigt. En cas de test positif, la personne doit être orientée vers une structure dédiée afin de réaliser un test de confirmation (ELISA). Si le TROD est négatif, la personne doit être informée des limites du test et orienté, si nécessaire, vers une structure dédiée.
DIAGNOSTIC DIRECT
La détection et la quantification de l’ARN génomique viral à partir d’un prélèvement sanguin sur tube EDTA (éthylène diamine-tétraacétique) par RT-PCR quantitatives sont indispensables afin de poser le diagnostic d’hépatite C active, d’orienter le patient vers un traitement et d’évaluer l’efficacité de celui-ci. L’infection C chronique est caractérisée par la présence de l’ARN viral pendant plus de 6 mois.
OUTILS DE DIAGNOSTIC NON VIROLOGIQUES
Le dosage de l’activité sérique de l’ALAT peut être envisagé pour le suivi mais avec des fluctuations au cours du temps. L’évaluation de l’activité de l’hépatite et de la fibrose hépatique peut-être effectuée de deux manières :
▶ une méthode non invasive, le Fibroscan®, qui mesure l’élasticité du foie par impulsion ultrasonore ;
▶ des nombreux biomarqueurs à partir d’une prise de sang qui permettent de déterminer un score (Fibrotest®, AST to Platelet Ratio Index ou APRI…). Le stade de fibrose est évalué par un score Métavir de F0 (pas de fibrose) à F4 (cirrhose) et A0 à A3 (inflammation).
| Points clés Le diagnostic d’une infection par le HCV repose avant tout par la recherche des anticorps anti-HCV. En cas de résultat positif, une évaluation par des techniques de diagnostic direct est réalisée. |
TRAITEMENT
Le traitement du HCV a connu une révolution au cours des années 2010 avec l’arrivée des premiers agents antiviraux directs (AAD). Les traitements historiques à base d’interféron alpha pegylé et de ribavirine ont été abandonnés. Contrairement aux infections par le HBV ou le HIV, le HCV est éradicable (guérison définitive) par le traitement antiviral (pas de latence possible car génome ARN uniquement). La guérison est caractérisée par un ARN viral indétectable 3 mois après l’arrêt du traitement. Le terme de réponse virologique soutenue (RVS) est utilisé. L’objectif du traitement antiviral est d’améliorer la qualité de vie, la survie des patients en empêchant la progression de la maladie vers la cirrhose, mais aussi de diminuer la contagiosité dans la population.
Tous les patients atteints d’une hépatite C chronique sont éligibles à ces traitements. Les traitements associent désormais 2 classes thérapeutiques au minimum parmi :
▶ les inhibiteurs de la protéase NS3/4A, affixe « -prévir » : grazoprévir, glécaprévir, voxilaprévir ;
▶ les inhibiteurs de la protéine NS5A, affixe « -asvir » : lédipasvir, velpatasvir, elbasvir, pibrentasvir ;
▶ les inhibiteurs de la polymérase NS5B, affixe « -buvir » : inhibiteurs nucléosidiques (sofosbuvir).
Les combinaisons thérapeutiques sont désormais des traitements combinant plusieurs molécules d’une même firme pharmaceutique avec une activité pangénotypique, excepté pour le Zepatier®.
▶ Epclusa® : sofosbuvir + velpatasvir (génotype 1 à 7)
▶ Mavyret® : glécaprévir + pibrentasvir (génotype 1 à 7)
Ces combinaisons thérapeutiques sont conditionnées sous forme de comprimés avec 1 prise par jour sur une durée de traitement de 2 à 3 mois avec une efficacité importante (RVS de plus de 90 %). Les effets secondaires sur ces schémas thérapeutiques courts sont limités.
| Points clés L’infection à HCV est une maladie curable par les traitements antiviraux désormais très efficaces sur une durée de traitement de 3 mois. |
PRÉVENTION
En l’absence de vaccin pour le HCV, la prévention repose sur un dépistage massif tout particulièrement dans les populations à risque de transmission, mais également sur des campagnes de prévention et la promotion d’utilisation de matériel à usage unique (toxicomanie). La sécurisation virale des dons de cellules, tissus (sang) et organes est systématiquement effectuée.
