Le virus de l’hépatite B (HBV ou VHB) est un virus à tropisme essentiellement hépatique pouvant être responsable d’hépatites aiguës et chroniques, de cirrhoses et d’hépatocarcinomes (cancers primitifs du foie). Le réservoir est strictement humain. Il est souvent présent en grande quantité dans le sang (≥ 108 particules/mL) et sa transmissibilité est très élevée (100 fois supérieure à celle du HIV [virus de l’immunodéficience humaine]). La répartition de l’infection à HBV est mondiale avec une plus forte prévalence dans les pays du Sud. Elle est estimée mondialement à 250 millions de sujets infectés (porteurs) et conduit à environ 900 000 décès par an.
CARACTÉRISTIQUES VIROLOGIQUES
TAXONOMIE
C’est un virus à ADN possédant une transcriptase inverse.
▶ Famille : Hepadnaviridae.
▶ Genre : Orthohepadnavirus.
▶ Espèce : Hepatitis B Virus (HBV).
▶ 10 génotypes.
GÉNOME
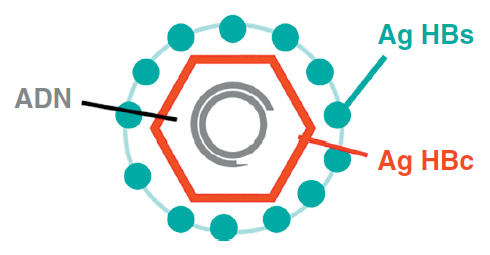
Le génome du HBV est un ADN (acide désoxyribonucléique) circulaire de petite taille (3,2 kb). Deux de ses particularités sont d’avoir des cadres de lecture chevauchants et d’être double brin partiel dans la particule virale (ou virion) (figure III.8.1).
PROTÉINES VIRALES
Les particules virales sont enveloppées. Elles sont polymorphes avec :
▶ des particules défectives et composées uniquement de l’enveloppe virale porteuse de protéines S, très majoritaire ;
▶ des particules complètes et infectieuses (dites particules de Dane), composées de nucléocapsides icosaédriques enveloppées et porteuses de protéines S.
a) La protéine S ou antigène HBs (Ag [antigène] HBs) : c’est la glycoprotéine de surface (S) de la particule virale. Elle est reconnue par les anticorps neutralisants et est utilisée comme antigène vaccinal.
b) La protéine C ou antigène HBc (Ag HBc) : c’est la protéine de capside (C). Elle n’est pas détectable dans le sang. Elle induit la production d’anticorps non-protecteurs, témoins d’une infection par HBV.
c) La protéine E ou antigène HBe (Ag HBe) : ce polypeptide est obtenu par clivage d’un précurseur protéique de la protéine C (préC) et est normalement libéré dans le sang en cas de réplication virale intense. Certaines mutations peuvent bloquer sa production et son excrétion sanguine. Elle n’est pas indispensable au virus et pourrait avoir un rôle tolérogène. Elle induit la production d’anticorps non-protecteurs témoins d’une infection par HBV.
d) La protéine P ou polymérase : c’est une transcriptase inverse intervenant dans la synthèse du génome viral (ADN circulaire double brin) à partir d’ARN (acide ribonucléique) prégénomiques.
e) La protéine HBx : c’est une protéine transactivatrice intervenant dans la régulation de l’expression du génome viral (réplication) et parfois humain (oncogenèse).
TROPISME ET RÉPLICATION
HBV infecte principalement les hépatocytes. Le virus se fixe au récepteur cellulaire (NTCP [Na+-Taurocholate Co-transporting Polypeptide]) grâce à l’Ag HBs, ce qui induit une endocytose. La nucléocapside migre ensuite vers un pore nucléaire et libère le génome viral dans le noyau. Ce génome persiste sous la forme d’un épisome (génome viral ADN double brin circulaire complet superenroulé [cccDNA, pour covalently close circular DNA]) qui permet l’expression des protéines virales. Les protéines C s’assemblent avec l’ARN prégénomique pour former des nucléocapsides qui bourgeonnent pour acquérir l’enveloppe virale porteuse d’Ag HBs avant d’être excrétées. L’ARN prégénomique est rétrotranscrit en ADN double brin partiel. La réplication virale est très intense avec plusieurs milliards de particules virales produites journellement (figure III.8.2).
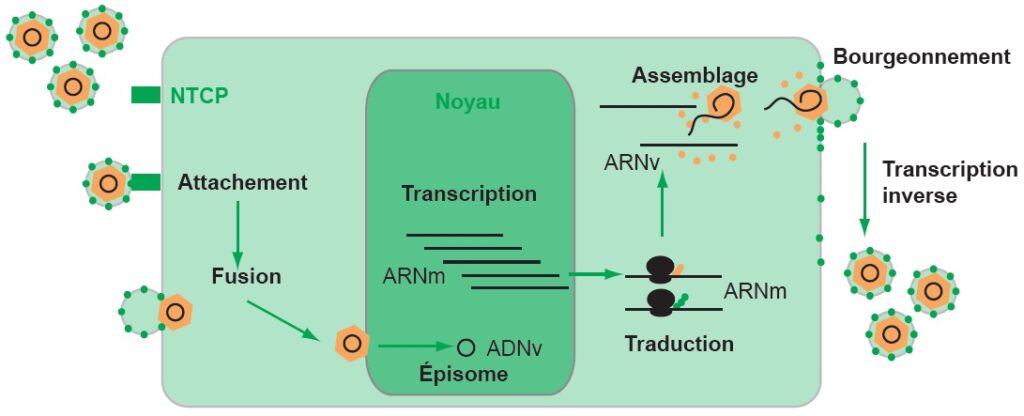
ADN : acide désoxyribonucléique ; ARN : acide ribonucléique ; NTCP : Na+-Taurocholate Co-transporting Polypeptide.
| Points clés HBV est un petit virus enveloppé à ADN. Il est hépatotrope et possède une transcriptase inverse. Le génome épisomal peut être latent dans les noyaux des hépatocytes. |
DONNÉES ÉPIDÉMIOLOGIQUES
La répartition de l’infection à HBV est mondiale. On estime qu’environ 250 millions de personnes sont infectées de par le monde. En France, on estime à 135 000 le nombre de sujets chroniquement infectés, soit une prévalence de 0,3 %. L’incidence des hépatites B aiguës en France est de 300 cas/an. L’hépatite B aiguë est une maladie à déclaration obligatoire en France. On définit des zones géographiques de haute endémicité (Afrique subsaharienne, Asie du Sud-Est avec un risque de contamination > 60 % au cours d’une vie) et des zones de faible endémicité (risque d’infection < 20 % au cours d’une vie). Bien qu’enveloppé, le virus est très résistant.
Les modes de transmission sont multiples :
▶ transmission mère – enfant (TME [transmission mère-enfant]), principalement lors du travail et de l’accouchement mais aussi via l’allaitement et possiblement le maternage. Elle est majoritaire dans les pays de haute endémicité et conduit fréquemment à des infections chroniques chez le nouveau-né (≥ 90 %) en l’absence de prophylaxie ;
▶ transmission sexuelle, favorisée par les partenaires multiples. L’infection à HBV est une infection sexuellement transmissible (IST). Le virus est présent dans les sécrétions génitales ;
▶ transmission parentérale via le sang en particulier (essentiellement toxicomanie intraveineuse, très rarement transfusion ou produits dérivés du sang). Des cas de transmissions par accident d’exposition au sang (AES), actes invasifs, soins dentaires, acupunctures, piercings ou tatouages existent ;
▶ transmission inconnue via l’entourage familial ou en collectivité. Elle reste très minoritaire. Le virus est détecté dans de nombreux liquides biologiques dont la salive (transmission discutée) et pourrait être transmis par le partage d’objets de toilette en particulier.
| Points clés Les infections à HBV sont principalement transmises par voie sexuelle (IST) en Europe. Dans les pays de haute endémicité, la transmission est essentiellement mère – enfant et conduit à des infections chroniques. |
PHYSIOPATHOLOGIE ET MANIFESTATIONS CLINIQUES HBV
est un virus peu cytolytique. C’est principalement la réponse immune de l’hôte qui est responsable de l’hépatite et de sa sévérité.
Une réponse immune adaptée conduit à un contrôle en quelques semaines de la réplication virale avec des hépatites aiguës symptomatiques ou asymptomatiques. Le virus peut persister sous forme épisomale (hépatite occulte) et être éventuellement réactivé en cas de traitement immunodépresseur (environ 10 %).
Une réponse immune insuffisante conduit soit à une tolérance (infection réplicative sans cytolyse et donc sans hépatite), soit à une hépatite chronique (infection réplicative avec cytolyse et donc hépatite).
À l’inverse, une réponse incontrôlée peut conduire à une hépatite fulminante conduisant par destruction rapide du foie (cytolyse majeure) à une insuffisance hépatocellulaire aiguë diagnostiquée par une chute de l’activité du complexe prothrombinique (< 30 %), une hyperammoniémie et une encéphalite hépatique. Ces formes sont rares, 1–2 % des contaminations, mais souvent létales (50 %). HBV est le virus des hépatites donnant le plus d’hépatites fulminantes. La durée d’incubation est variable (60–110 j). Lors des hépatites B aiguës, les principales manifestations cliniques sont une asthénie, une anorexie et un ictère cutanéo-muqueux d’intensité variable. Ces signes peuvent être associés à une décoloration des selles et à une coloration des urines. Ces modifications sont liées à la réduction de l’élimination de la bilirubine conjuguée dans la bile et donc dans les selles (stercobiline), la bilirubine sanguine étant alors éliminée par voie urinaire (urobiline). On peut également parfois noter un prurit généralisé lié au passage des sels biliaires dans la circulation sanguine.
Une hépatite B chronique est définie par la persistance des marqueurs viraux directs pendant plus de 6 mois (en pratique Ag HBs dans le sérum). Les hépatites B chroniques peuvent conduire à des cirrhoses (> 20 % à 20 ans) et les cirrhoses sont un terrain favorisant les carcinomes hépatocellulaires (CHC, incidence de 3–4 %/an sur cirrhose). HBV est donc un virus à potentiel oncogène.
Du fait de la persistance de cccDNA dans les hépatocytes sur de très longue durée même après guérison au stade aigu, des réactivations biologiques (reprise de réplication et production virales) et cliniques (hépatite) peuvent survenir post-guérison chez les immunodéprimés. Ceci conduit à la surveillance par sérologie et PCR (Polymerase Chain Reaction) de ces patients et même parfois à un traitement préventif.
Des manifestations extrahépatiques non spécifiques et dysimmunitaires sont possibles (syndrome de Guillain-Barré, périartérite noueuse, glomérulonéphrite…) (figure III.8.3).
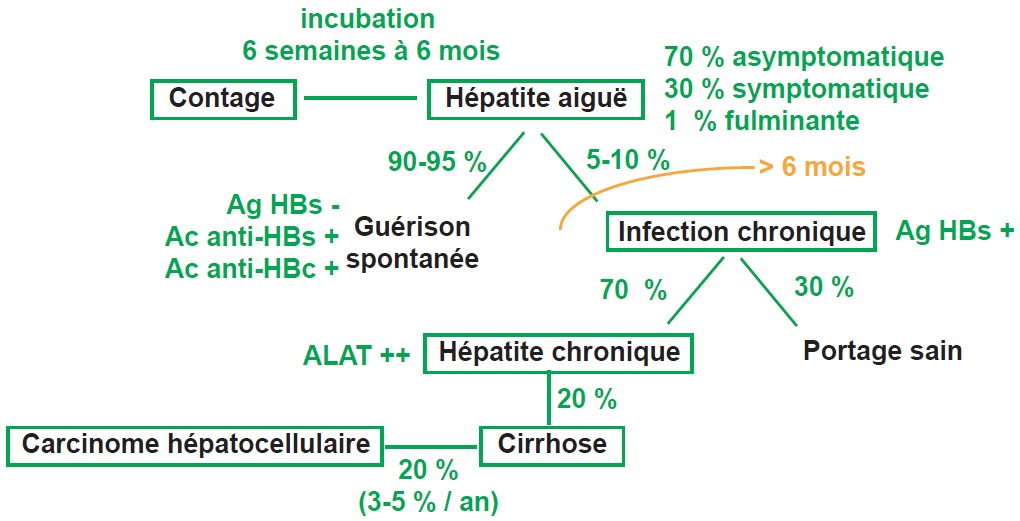
Ac : anticorps ; Ag : antigène ; ALAT : alanine aminotransférase.
| Points clés La sévérité de l’atteinte hépatique dépend principalement de la réponse immune de l’hôte. La clinique n’est pas spécifique mais commune à toutes les hépatites. Le risque principal est l’hépatite chronique qui peut conduire à une cirrhose et à un hépatocarcinome. |
DIAGNOSTIC
Le diagnostic est principalement biologique car les hépatites sont majoritairement asymptomatiques et d’étiologies multiples (toxique, médicamenteuse, auto-immune, infectieuse). Le dépistage de l’infection par HBV repose sur la sérologie détectant dans le sérum ou le plasma l’Ag HBs, les Ac anti-HBc et les Ac anti-HBs. Le diagnostic d’infection en cours repose sur le diagnostic direct avec la mise en évidence par EIA (Enzyme Immuno Assay) de l’Ag HBs sanguin (sérum ou plasma).
Le dépistage doit concerner les groupes à risque :
▶ personnes nées en zone de moyenne ou de haute prévalence du HBV ;
▶ partenaires sexuels d’un porteur d’Ag HBs ;
▶ consommateurs de drogue par voie intraveineuse ;
▶ personnes vivant sous le même toit qu’un porteur d’Ag HBs ;
▶ hémodialysés ;
▶ sujets séropositifs pour HIV et/ou HCV (virus de l’hépatite C) ;
▶ sujets ayant un antécédent d’IST ;
▶ lors de la découverte d’une augmentation des transaminases (AALAT [alanine aminotransférase] > ASAT [aspartate aminotransférase]) ;
▶ déclaration de grossesse (prévention de la TME) ;
▶ sécurisation virale.
Les marqueurs sériques et leurs intérêts respectifs : (figures III.8.4A et B)
En dépistage :
▶ Ag HBs : signe la présence du HBV dans le sang et donc l’infection en cours ;
▶ Ac anti-HBs : signe une immunité protectrice si le taux est > 10 UI/mL (post-infectieuse ou post-vaccinale), > 100 UI/mL pour les professionnels de santé (car prédit une persistance d’un titre protecteur pendant une longue période) ;
▶ IgM anti-HBc : immunité en faveur d’une infection récente si à des titres importants (primo-infection).
En cas de dépistage positif :
▶ Ac anti-HBc totaux : signe une immunité post-infectieuse ou en cours d’infection ;
▶ AAg HBe : marqueur d’évolution de l’infection (attention, en cas de mutant préC, l’Ag HBe reste négatif même en présence d’une réplication virale importante) ;
▶ Ac anti-HBe : marqueur d’évolution de l’infection apparaissant souvent à distance de la contamination, en faveur d’une réplication virale faible (sauf en cas de mutant préC) ;
▶ HBV (charge virale HBV) : seul marqueur de réplication ; et permet la quantification du niveau de la réplication virale puisqu’il est détecté dans le plasma ou sérum par PCR en temps réel (suivi thérapeutique) (figure III.8.4A et B) ;
▶ augmentation de l’atteinte hépatique :
▪ élévation des ALAT (> ASAT) en faveur d’une cytolyse hépatique (suivi),
▪ activité du complexe prothrombinique (facteur pronostic),
▪ évaluation de la fibrose et de l’inflammation hépatique : score Métavir/Fibrotest®/Fibroscan®.
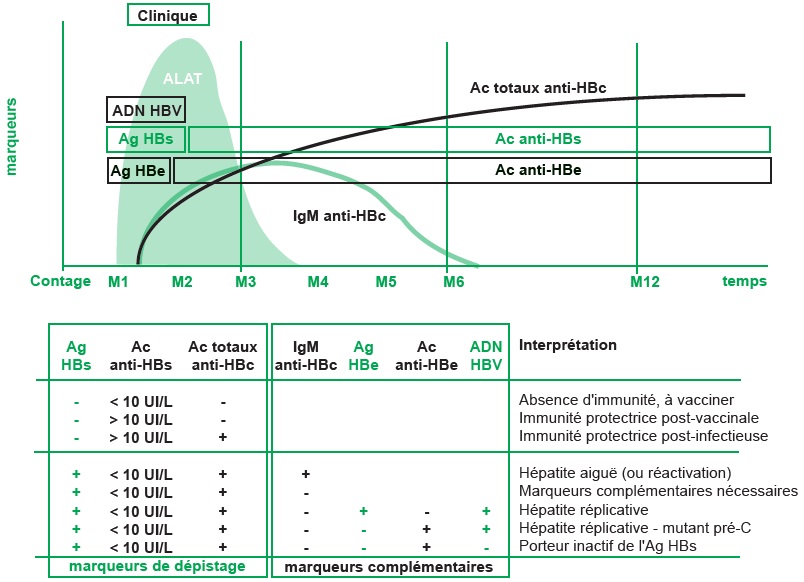
Ac : anticorps ; ADN : acide désoxyribonucléique; Ag : antigène ; ALAT : alanine aminotransférase ; HBV : virus de l’hépatite B ; IgM : immunoglobuline M.
| Points clés Le diagnostic virologique est basé sur le dépistage associant 3 marqueurs sanguins : Ag HBs, Ac anti- HBs et Ac anti-HBc. En cas d’infection (Ag HBs +), des marqueurs complémentaires sont réalisés (IgM [immunoglobuline M] anti- HBc avec déclaration obligatoire si +, Ag HBe et Ac anti-HBe, ADN HBV) pour caractériser l’infection et sa réplication. |
TRAITEMENT
▶ Traitement de l’hépatite aiguë à HBV :
▪ pas de traitement antiviral spécifique du fait de la fréquence très élevée des guérisons spontanées (arrêt des boissons alcoolisées et des médicaments hépatotoxiques non indispensables mais recommandé en cas d’hépatite B sévère) ;
▪ traitement symptomatique (repos, hydratation…) ;
▪ surveillance des sérologies (apparition des Ac anti-HBs) et des fonctions hépatiques (ALAT et taux de prothrombine).
▶ Traitements de l’hépatite fulminante :
▪ transplantation hépatique en urgence ;
▪ traitement possible par inhibiteur de la polymérase virale ;
▪ traitement symptomatique (réanimation).
▶ Traitements de l’hépatite chronique : le but est de contrôler la réplication virale et d’arrêter l’évolution des lésions hépatiques vers la cirrhose et, si possible, d’induire une immunité permettant au patient un contrôle de la réplication virale.
En pratique, les objectifs des traitements sont multiples.
▶ Objectif virologique : rendre l’ADN HBV indétectable dans le sang.
▶ Objectif biochimique : normaliser les ALAT.
▶ Objectif immunitaire :
• idéalement : disparition de l’Ag HBs, séroconversion HBs (apparition des Ac anti-HBs) signant la guérison, mais difficile et long à obtenir avec les antiviraux actuels : quasi-absence de négativation de l’Ag HBs ;
• plus réaliste, pour les patients avec un Ag HBe : séroconversion HBe (apparition des Ac anti-HBe).
▶ Objectif histologique : améliorer l’histologie hépatique (inflammation et fibrose) avec une réversion partielle de la fibrose.
On peut utiliser :
▶ les inhibiteurs nucléosidiques de la transcriptase inverse du HBV (ténofovir ou entécavir per os) : bonne tolérance, monothérapie avec traitement à vie ;
▶ l’interféron alpha pegylé : traitement à durée limitée (48 semaines, 1 ISC [injection sous-cutanée]/semaine) avec une tolérance moyenne (efficacité génotype dépendante). Indications limitées.
| Points clés Seules les hépatites B chroniques font l’objet d’un traitement antiviral. Celui-ci permet de bloquer la réplication virale et l’évolution vers la cirrhose, mais permet rarement la guérison. |
PRÉVENTION
La prévention des infections à HBV pour la population générale est basée sur la vaccination obligatoire du jeune enfant.
▶ La vaccination est obligatoire pour les jeunes enfants (injection à 2 mois, 4 mois et 11 mois) et les professionnels de santé. Elle est recommandée pour la population générale.
▶ D’autres schémas sont utilisables dans des cas particuliers. Par exemple : nouveau-né de mère Ag HBs positif : 3 doses selon le schéma 0, 1, 6 mois.
Indications particulières :
▶ professionnelle (profession de santé, sécurité et secours) ;
▶ médicale (hémophiles, dialysés, polytransfusés, transplantés) ;
▶ nouveau-né de mère porteuse de l’Ag HBs : justifie le dépistage obligatoire à 6 mois de grossesse. Sérovaccination à la naissance (immunoglobulines anti-HBs et vaccin) ;
▶ Recherche de l’Ag HBs obligatoire au plus tard à 6 mois de grossesse ; mais le dépistage des femmes enceintes est recommandé lors de la première consultation de déclaration de grossesse pour une initiation précoce d’un traitement antiviral anti-HBV en cours de grossesse et une sérovaccination du nouveau-né à l’accouchement ;
▶ accident d’exposition au sang (AES) ou exposition sexuelle : sérovaccination en absence de protection vaccinale (Ac anti-HBs) ;
▶ sécurisation virale des tissus humains (sang, tissus, organes) ;
▶ lutte contre les IST (multipartenariat, préservatifs) ;
▶ lutte contre la toxicomanie intraveineuse et mise à disposition de kits d’injection stériles ;
▶ surveillance accrue de la réactivation virale chez les personnes avec des Ac anti-HBc et les immunodéprimés (traitement immunosuppresseur, chimiothérapie, anti-CD20…) ;
▶ maladie à déclaration obligatoire (sujet Ag HBs + et IgM anti-HBc +).
